youtu.be
これ見て。
もしかしたら、前エントリでも書いているのですが、まあ、知らない人いるよな(副作用をいう人が大体その辺りを踏まえて喋っていないので)と思います。
ワクチンの副作用は、「予期される副作用」です
小林製薬の紅麹は、予期されていない副作用です。というかまあ、そもそもそういう事の収集をちゃんとしているか怪しいのです。
医薬品に関しては、販売前から副作用は蓄積しており、治験期間中のものも含めて定期的に厚生労働省に報告までが義務です。因果関係等も、現場の医師の判断・製薬会社の判断が見られ、「因果関係が明らかに否定できる」以外は因果関係は想定されます。
ワクチンも副作用は収集されていて、我々も見る事が可能です。
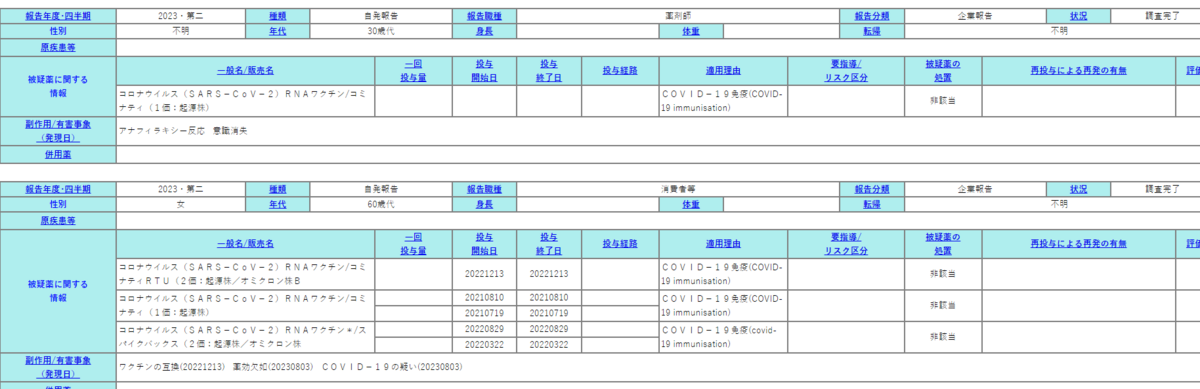
国が認可した薬については、副作用被害救済制度が設定されている。
この辺りでなのですが、国としても制度があります。これは、薬害の裁判の歴史より、補償等が長いあいだ受けられなかったという事を踏まえ、設けられた制度になります。
https://www.mhlw.go.jp/file/06-Seisakujouhou-11120000-Iyakushokuhinkyoku/0000185081.pdf
「薬を無茶苦茶に使った」「医療機関のミスの場合にはこの制度が利用出来ない」のでご注意下さい。
ワクチンに関しては「予防接種後健康被害救済制度」という名前になります。新型コロナウィルスワクチンについても適用になりますのでご確認下さい。
無論、万能ではないし万全ではないのだが、医療関係での「大学の先生」はあんまり信用しない方がいい。
とは思ってます。まあ、これは私が、治験業界に長くいるからというのもあるのですが。
日本のお医者さんで、臨床は知ってるし研究も知っている方は多いですが、医薬行政に関してはかなり理解してません。偉い先生も大体はワクチンの治験を実施してないかと思います。そういうふわっとした先生が大量動員されてたのが今回の新型コロナウィルスの周りで、コメンテーターみたいに出てきていたのがもうね・・・・・・
規制当局がかけてる規制もあんま知られてない。
主にはFDA主導なんですが、医薬品には、治験だとGCP/製造だとGMP/臨床研究(動物実験)だとGLP/製造販売後調査でGPSP/安全性管理とかでGVP、他電子データの保存の仕方であったりとか、様々に当局規制があります。
もう高い本が何冊もあるような。コンサルが仕事にしてるような。コンサルも健康食品辺りだとええ加減な気もしますが、工場建てるのにその審査の準備だけで一年二年経つくらいです。
だからまあ、健康食品の場合には、絶対軽くは行われているとは思います。原料の工場まで自分等でちゃんと見て管理を確認する事まで強制されるので、とにかく重いんですよね。まあ、ジェネリック医薬品で事件起こった訳ですが、審査の目が届かないところではGMP違反でごまかしたくなるのは分かります。例えば100錠分作るとして、釜とかで練ってる時に分量が減ったりして想定より減りすぎてしまった場合に、継ぎ足しは認められてないんですよね。ここで原料継ぎ足しというのが結構発生してたりします。違反です。
睡眠導入薬混入の際も、「これ問題視したらロット全部廃棄」というのが怖くてやらなかったんでしょう。一番はその釜共用で、年間で計画的に生産しないといけなくて、もう一度やり直すとかが時間的に厳しいとかあるわけです。ジェネリックの工場は、生産能力の限界に近いところまで使われてまして、効率よく計画する最適化計画用のソフトも結構高いんですが導入されているんで、バッファを削りすぎた結果だと思います。
治験業界の、私がいるような会社も、結局のところ、コストダウンの為の存在のようなものでして、専門性の割に給料は~とか言われがち、日本ってそんな会社がめっちゃあるんですよね・・・・・・まあ、海外でもそうなんすけど。